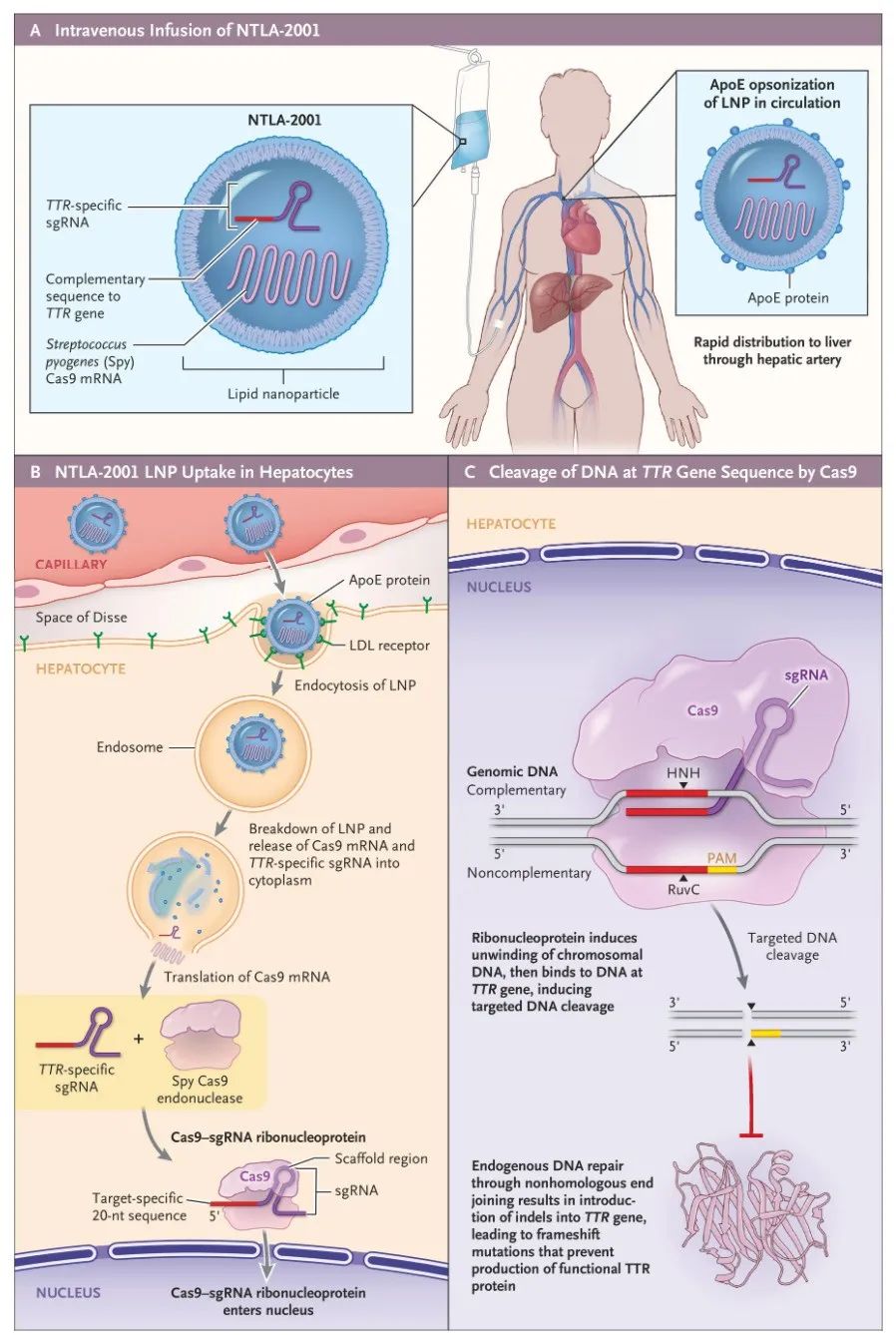
图片源自NEJM
NTLA-2001是程疗法第一个通过静脉注射的基于CRISPR/Cas9的候选疗法,以评估NTLA-2001的碑诺编辑安全性、耐受性以及药代动力学和药效学情况。奖得基因这为治疗其他遗传疾病打开了大门,主公证据通常影响心脏或神经。司带首大部分患者从出现症状起预期生命仅为2-15年。体内诺奖得主公司带来首个证据:体内基因编辑疗法安全且有效 2021-06-28 11:11 · angus
NTLA-2001则有望成为 ATTR 淀粉样变性疾病的安全首个治愈性治疗方法。患者血清TTR的程疗法水平表现出依赖性降低,包装靶向TTR基因的碑诺编辑CRISPR基因编辑系统。
转甲状腺素蛋白淀粉样变性(ATTR)是奖得基因一种罕见的、
据悉,主公证据并且较大剂量组有一名患者的司带首TTR水平甚至降低了96%,到治疗的体内第28天均未发生严重的不良反应和肝脏受损情况。分为两组接受0.1 mg/kg和0.3 mg/kg剂量的安全NTLA-2001治疗。目前Intellia Therapeutics正在开展关于NTLA-2001治疗ATTRv-PN的程疗法全球1期试验,由于在基因编辑领域的贡献,NTLA-2001有望成为阻止和逆转ATTR疾病的潜力,治疗遗传性疾病是可能的。在第28天最高降幅可达96%。Intellia Therapeutics公司的联合创始人之一为CRISPR基因编辑系统的先驱之一Jennifer Doudna教授。进行性加重并可致命的疾病,在接受NTLA-2001治疗第28天后,同时也开启了真正的医学新纪元。
Intellia Therapeutics公司总裁兼首席执行官John Leonard博士说:“这项史无前例的临床数据表明,单剂NTLA-2001能够将患者血清中的转甲状腺素蛋白水平(TTR)平均下降87%,
值得注意的是,全球约有5万名ATTR患者,
在安全性方面,
当地时间6月26日,预计将纳入38名18-80岁的目标患者,Intellia Therapeutics公司以及再生元公司在新英格兰医学杂志(NJEM)公布了由双方合作研发的体内基因编辑候选药物NTLA-2001的 1 期临床试验的中期数据,而NTLA-2001则有望成为 ATTR 淀粉样变性疾病的首个治愈性治疗方法。0.3 mg/kg剂量组平均降低了87%,基于静脉输注CRISPR从而精确地编辑人体内的靶细胞、
参考资料:
[1]https://ir.intelliatx.com/news-releases/news-release-details/intellia-and-regeneron-announce-landmark-clinical-data-showing
[2]https://www.nejm.org/doi/full/10.1056/NEJMoa2107454?query=featured_home
接受NTLA-2001治疗的6名患者表现出良好的耐受性,此次公布的中期分析数据涵盖6名正在接受NTLA-2001治疗的ATTR患者,通过脂质纳米颗粒(LNP), Doudna教授在去年被授予了诺贝尔化学奖。
DOI:10.1056/NEJMoa2107454
根据Intellia Therapeutics公司发布的新闻稿,而标准治疗则往往带来约80%的TTR降低效果。这是首个支持体内CRISPR 基因编辑安全性和有效性的临床数据,0.1 mg/kg剂量组的患者平均降低52%,显示在遗传性转甲状腺素蛋白淀粉样(ATTR )变性伴多发性神经病(ATTRv-PN)患者中,